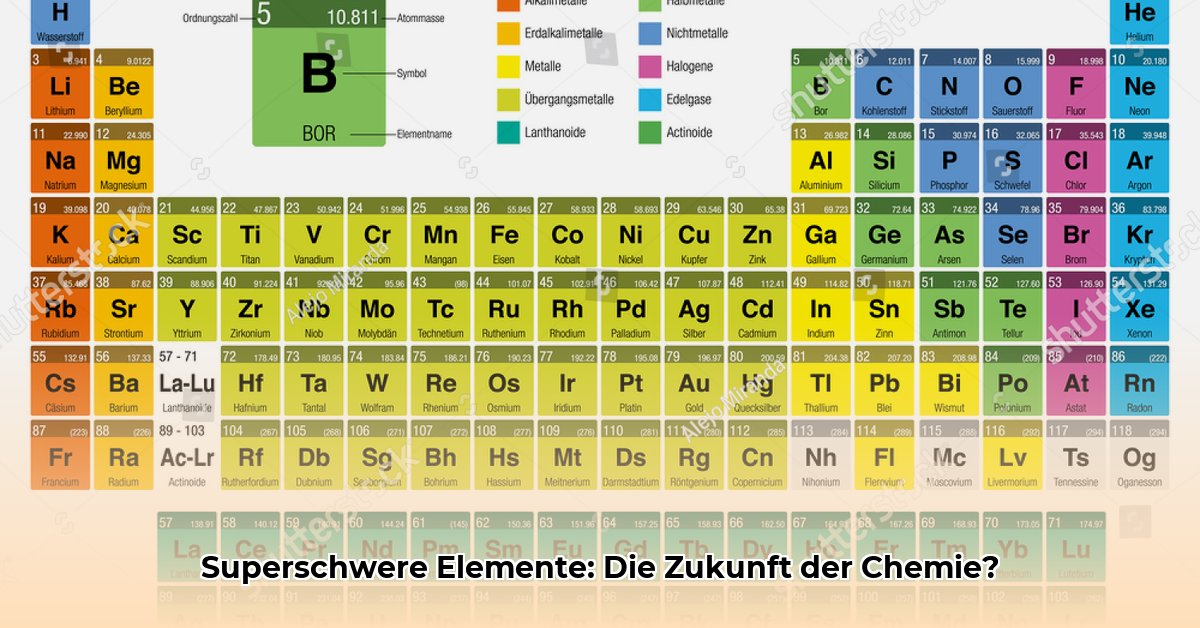
Periodensystem der Elemente: Eine Reise durch die Welt der Atome
Stellen Sie sich vor: eine Tabelle, die alle Bausteine unserer Welt, jedes einzelne chemische Element, übersichtlich ordnet. Das ist das Periodensystem der Elemente – keine trockene Auflistung, sondern eine spannende Geschichte von Entdeckungen, genialen Einsichten und ungelösten Rätseln. Von Wasserstoff, dem leichtesten Element, bis hin zu den flüchtigen, künstlich erzeugten Superschweren – alle sind hier vereint. Wie entstand diese geniale Ordnung? Und was verbirgt sich hinter den geheimnisvollen Superschweren Elementen, die Forscher mit Hochdruck suchen? Begeben wir uns auf eine Entdeckungsreise in die faszinierende Welt der Atome! Wussten Sie beispielsweise, dass die Vorhersage unbekannter Elemente durch das Periodensystem zu einigen der wichtigsten Entdeckungen in der Chemie führte?
Das Periodensystem: Struktur und Organisation
Das Periodensystem ist in Zeilen (Perioden) und Spalten (Gruppen) gegliedert. Jedes Kästchen repräsentiert ein Element mit seinen einzigartigen Eigenschaften. Elemente innerhalb einer Gruppe ähneln sich in ihrem chemischen Verhalten, weil sie die gleiche Anzahl von Außenelektronen (Valenzelektronen) besitzen – die "Hände", mit denen Atome Verbindungen eingehen. Die Elektronenkonfiguration ist gewissermaßen der "Fingerabdruck" eines Elements. Können Sie sich vorstellen, wie wichtig dieses Prinzip für das Verständnis chemischer Reaktionen ist?
Innerhalb der Perioden ändern sich die Eigenschaften der Elemente systematisch. Der Atomradius (die Größe des Atoms) nimmt beispielsweise von links nach rechts ab, während die Elektronegativität (die Fähigkeit, Elektronen anzuziehen) zunimmt. Diese „periodischen Trends“ sind für die Chemie und die Entwicklung neuer Materialien fundamental. Wie beeinflusst die periodische Anordnung die Eigenschaften von Metallen im Vergleich zu Nichtmetallen?
Die Geschichte des Periodensystems: Mendelejew und die Vorhersage der Zukunft
Im 19. Jahrhundert, als das Wissen über Atome noch in den Kinderschuhen steckte, entdeckten Dmitri Mendelejew und Lothar Meyer unabhängig voneinander bemerkenswerte Muster. Sie ordneten die bekannten Elemente nach ihrer Atommasse und stellten fest, dass sich ähnliche Eigenschaften periodisch wiederholten – ein regelmäßiger Tanz der Elemente. Mendelejews Genie zeigte sich besonders in seinem Mut, Lücken in seinem System zu lassen. Er prognostizierte die Existenz noch unbekannter Elemente und ihre Eigenschaften – mit erstaunlicher Genauigkeit! Wie hat diese vorausschauende Denkweise die weitere Entwicklung der Chemie beeinflusst?
Superschwere Elemente: Am Rande des Möglichen
Am Ende des Periodensystems, jenseits der bekannten, stabilen Elemente, liegen die superschweren Elemente. Diese werden nicht in der Natur gefunden, sondern in aufwendigen Experimenten mit Teilchenbeschleunigern künstlich erzeugt. Ihre Existenz ist flüchtig – sie zerfallen oft innerhalb von Sekundenbruchteilen. Trotzdem sind sie für Wissenschaftler enorm interessant. Ihre Erforschung erlaubt es uns, fundamentale Prinzipien der Physik zu testen, wie beispielsweise die Auswirkungen der Relativitätstheorie auf das Verhalten von Atomen. Die Synthese und Analyse dieser Elemente stellt eine immense technische und wissenschaftliche Leistung dar. Welche Herausforderungen birgt die Erforschung dieser kurzlebigen Elemente?
Anwendungen und Zukunftsperspektiven
Das Periodensystem ist kein abstraktes Konzept; es ist die Grundlage unzähliger Anwendungen in unserem Alltag. Medikamente, Smartphones, Autos, Solarzellen – all das basiert auf dem Verständnis der Elementeigenschaften. Die Möglichkeiten der modernen Technik sind untrennbar mit dem Wissen um das Periodensystem verbunden.
Auch die superschweren Elemente, trotz ihrer Kurzlebigkeit, könnten zukünftige Anwendungen bergen. Experten spekulieren über einzigartige Eigenschaften, die in der Materialwissenschaft, Medizin oder Energietechnik nützlich sein könnten. Allerdings steckt die Forschung hier noch in den Kinderschuhen. Welche revolutionären Materialien könnten durch das Verständnis superschwerer Elemente entstehen?
Synthese superschwerer Elemente: Herausforderungen und zukünftige Anwendungen
Die Herstellung superschwerer Elemente ist eine immense Herausforderung. Leichtere Atomkerne werden mit beschleunigten Kernen beschossen, doch die Wahrscheinlichkeit der erfolgreichen Synthese eines superschweren Elements ist extrem gering. Es ist wie die Suche nach einer Nadel im Heuhaufen – nur dass der Heuhaufen planetar ist und die Nadel nur für einen Sekundenbruchteil existiert.
Neue Techniken wie die Laser-Resonanz-Chromatographie (LRC) bieten vielversprechende Ansätze zur Detektion und Untersuchung dieser flüchtigen Elemente, ermöglichen eine höhere Empfindlichkeit und überwinden Limitationen bisheriger Methoden. Die LRC erlaubt die Analyse von einfach geladenen Lawrencium-Ionen (Element 103) und leichteren Homologen. Die Entwicklung und Verbesserung dieser Methode ist entscheidend für zukünftige Entdeckungen und ein tieferes Verständnis der „Insel der Stabilität“, einer hypothetischen Region im Periodensystem, in der superschwere Elemente eine unerwartet lange Lebensdauer aufweisen könnten. Welche Rolle spielt die LRC in der Erforschung der „Insel der Stabilität“?
Schlüsselerkenntnisse:
- Fortschritte in der Laser-Resonanz-Chromatographie (LRC) ermöglichen die Untersuchung von superschweren Elementen.
- Die LRC überwindet Limitationen der traditionellen optischen Spektroskopie.
- Zukünftige Anwendungen könnten neue Materialien und Fortschritte in der Nukleartechnologie ermöglichen.
Die Erforschung des Periodensystems, insbesondere der superschweren Elemente, ist ein spannendes Forschungsfeld voller Herausforderungen, aber auch mit dem Potenzial für bahnbrechende Entdeckungen. Die Zukunft der Chemie und vieler weiterer wissenschaftlicher Disziplinen hängt eng mit dem fortlaufenden Verständnis und der Nutzung der Elemente zusammen.